早在2016年美國(guó)國(guó)防部制造和加工中心(NCDMM)推動(dòng)的美國(guó)國(guó)家增材制造創(chuàng)新研究所America Makes開始與私營(yíng)非營(yíng)利性組織美國(guó)國(guó)家標(biāo)準(zhǔn)學(xué)會(huì)(ANSI)合作,為快速發(fā)展的3D打印行業(yè)制定標(biāo)準(zhǔn)和規(guī)范。

這兩個(gè)組織啟動(dòng)了制定3D打印標(biāo)準(zhǔn)的合作項(xiàng)目(AMSC),這是增材制造行業(yè)的一個(gè)監(jiān)管機(jī)構(gòu),其目標(biāo)是創(chuàng)建一個(gè)獨(dú)特的路線圖以確定必要的標(biāo)準(zhǔn),并協(xié)調(diào)和加速最終可行方法的開發(fā)過程。并且制定符合多方利益的需求的行業(yè)規(guī)范,促進(jìn)行業(yè)可持續(xù)的增長(zhǎng)。目前主要成立了設(shè)計(jì)材料 工藝 維護(hù)以及資格認(rèn)證方面,共設(shè)立4個(gè)工作組,起草文件編寫。AMSC增材制造標(biāo)準(zhǔn)化路線圖(版本1.0 )已于2016年12月向公眾發(fā)布以供審查和評(píng)論。
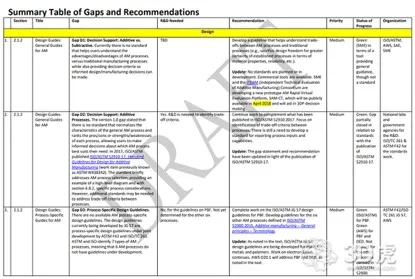
于此同時(shí)歐盟2015年也有類似計(jì)劃。歐盟為了對(duì)整個(gè)3D打印產(chǎn)業(yè)做一個(gè)整體規(guī)劃,對(duì)接德國(guó)《工業(yè)4.0》政策,進(jìn)而發(fā)布了最新“3D打印標(biāo)準(zhǔn)化路線圖”,以規(guī)整3D打印技術(shù)在發(fā)展戰(zhàn)略 中 的 位 置 及 方 向 。 在 歐 盟 地 七 框 架 計(jì) 劃 的 資 助 下 , 名 為 “3D 打 印 標(biāo) 準(zhǔn) 化 支 持 行 動(dòng)(SASAM)”的項(xiàng)目于2015年6月發(fā)布了一份3D打印標(biāo)準(zhǔn)化路線圖。

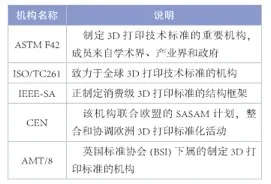
我國(guó)最近步伐也明顯加快,早在2014年我們國(guó)家就成立首個(gè)3D打印的評(píng)測(cè)中心,并加入了ISO/TC261國(guó)際標(biāo)準(zhǔn)化組織增材制造技術(shù)委員會(huì)。2016年全國(guó)增材制造標(biāo)準(zhǔn)化技術(shù)委員會(huì)成立,近期發(fā)布了我國(guó)首部《3D打印標(biāo)準(zhǔn)化白皮書2018》(以下簡(jiǎn)稱“白皮書”)。
今年5月,TPM3D的用戶之一–海爾集團(tuán)牽頭制定的3D打印國(guó)家標(biāo)準(zhǔn)——《增材制造(3D打印)工藝分類及原材料》正式在國(guó)家標(biāo)準(zhǔn)化管理委員會(huì)發(fā)布。
作為我國(guó)3D打印領(lǐng)域的第一項(xiàng)涵蓋全產(chǎn)業(yè)鏈的工藝原理和材料分類標(biāo)準(zhǔn),該標(biāo)準(zhǔn)建立起支撐3D打印技術(shù)發(fā)展最基礎(chǔ)的技術(shù)規(guī)范,從根本上解決了3D打印技術(shù)工藝原理和材料分類描述不統(tǒng)一的問題。據(jù)悉海爾的《增材制造(3D打印)技術(shù)云服務(wù)平臺(tái)模式規(guī)范》也正在報(bào)批中。
小編也收集到標(biāo)準(zhǔn)全文,加入文末SLS技術(shù)微信群,就可以看到。
還有消息表明:根據(jù)2018年第6號(hào)中國(guó)國(guó)家標(biāo)準(zhǔn)公告,由國(guó)家增材制造產(chǎn)品質(zhì)量監(jiān)督檢驗(yàn)中心(江蘇)牽頭制定的《增材制造主要特性和測(cè)試方法零件和粉末原材料》現(xiàn)已正式發(fā)布。將于2019年3月1日起正式實(shí)施。
在筆者關(guān)注的醫(yī)療器械方向:2018年2月,國(guó)家食品藥品監(jiān)督總局醫(yī)療器械技術(shù)評(píng)審中心公開征求《定制式增材制造醫(yī)療器械注冊(cè)技術(shù)評(píng)審指導(dǎo)原則》(征求意見稿)的意見。該指導(dǎo)原則涵蓋骨、關(guān)節(jié)、牙齒無源植入性醫(yī)療器械,關(guān)于產(chǎn)品性能:材料表征、陳品結(jié)構(gòu)和機(jī)械性能、生物相容性、清洗滅菌以及動(dòng)物試驗(yàn)和醫(yī)工交互條件:增材制造軟件設(shè)計(jì)、打印設(shè)備、工藝、后處理、原材料和終產(chǎn)品的測(cè)試,以及清洗、包裝和滅菌等方面進(jìn)行控制等進(jìn)行規(guī)定。目前我國(guó)有四款產(chǎn)品通過了3D打印的CFDA認(rèn)證,分別是:愛康醫(yī)療與北醫(yī)三院合作的3D打印髖臼杯、3D打印人工椎體、3D打印脊柱椎間融合器;邁普醫(yī)學(xué)3D打印硬腦(脊)膜補(bǔ)片,這對(duì)于制定醫(yī)療器械行業(yè)的3D打印標(biāo)準(zhǔn)提供了重要參考價(jià)值和經(jīng)驗(yàn)。

于此同時(shí),醫(yī)療康復(fù)矯形器(輔具)行業(yè)今年也有動(dòng)作。《3D打印矯形器設(shè)計(jì)、制造、使用標(biāo)準(zhǔn)與全流程監(jiān)管的專家共識(shí)》也已經(jīng)發(fā)表出來,對(duì)未來康復(fù)醫(yī)療事業(yè)也具有指導(dǎo)意義。

總結(jié):隨著行業(yè)規(guī)模越來越大,中國(guó)的3D打印事業(yè)標(biāo)準(zhǔn)化也逐漸規(guī)范并和國(guó)際接軌,這對(duì)于企業(yè)來說是挑戰(zhàn)也是機(jī)遇。而人們?cè)谑褂?D打印產(chǎn)品時(shí)也逐漸會(huì)有標(biāo)可參,有法可依了。

布會(huì)small-scaled.jpg)


金色簡(jiǎn)約現(xiàn)代風(fēng)新品發(fā)布會(huì)手機(jī)邀請(qǐng)函-1920-x-1080-像素.png)